Физические свойства воды
При обычных условиях вода — жидкое прозрачное вещество без цвета, вкуса и запаха. Плотность жидкой воды имеет максимальное значение 1 г/см3 при 4 °C. При 0 °C вода переходит из жидкого состояния в твёрдое — лёд. При 100 °C кипит и переходит в газообразное состояние — водяной пар. Аналоги воды по строению и химическому составу — H2S, H2Se, H2Te — при комнатной температуре находятся в газообразном состоянии. Если бы свойства воды подчинялись общей закономерности, то она закипала бы при температуре -70 °C, а лёд образовывался бы при -90 °C, что вряд ли способствовало жизни на планете в её настоящем виде. Наличие водородной связи у низкомолекулярного вещества воды и объясняет аномально высокие значения её температур плавления и кипения.
Чистое вещество вода обладает и другими особенностями, которые делают это соединение поистине уникальным.
Вода способна расширяться при замерзании и иметь при +4 °C максимальную плотность. Поэтому при температуре меньше +4 °C лёд занимает верхнюю часть водоёма, укрывая, как шубой, его нижние слои и защищая водоём от промерзания. Это спасает нашу планету от обледенения. Не обладай вода таким загадочным свойством, все водоёмы и даже Мировой океан за определённый геологический период промёрзли бы до дна. Жизнь на Земле не только не получила бы своего эволюционного развития, она просто бы не возникла.
Вода обладает высокими значениями удельной теплоты плавления и удельной теплоты парообразования, которым академик В. И. Вернадский придавал планетарное значение, так как они определяют многие физико-химические и биологические процессы на Земле (рис. 157).
Высокая удельная теплота плавления льда, равная 332 • 103 Дж/кг, оберегает нашу планету от всемирных потопов. Таяние льда (рис. 158) и снега связано с огромными энергетическими затратами, поэтому процесс происходит постепенно, в большинстве случаев не причиняя вреда природе.
 |
| Рис. 157. Облака — это миллиарды мельчайших капелек воды |
 |
| Рис. 158. Таяние льда |
На испарение 1 кг воды при нормальном атмосферном давлении и температуре кипения расходуется 2257 • 103 Дж теплоты, т. е. приблизительно в 7 раз больше, чем на плавление 1 кг льда. В этом причина сохранения воды в жидком состоянии на нашей планете. Даже в самые жаркие дни вода испаряется крайне медленно. Поэтому и сезоны года меняются не резко, а плавно: лето — осень — зима — весна.
Вода имеет высокую удельную теплоёмкость. Эта величина показывает, какое количество теплоты надо затратить для нагревания 1 кг воды на 1 K (рис. 159). Оказывается, оно равно 4,1868 • 103 Дж.
Из-за высокой удельной теплоёмкости воды на континентах не бывает резкого перепада температур зимой и летом, ночью и днём, поскольку они окружены гигантским регулятором, своеобразным термостатом — водами Мирового океана.
При нагревании всех веществ удельная теплоёмкость их, как правило, возрастает, но вода — исключение. Изменение удельной теплоёмкости воды с повышением температуры аномально: от 0 до 30 °C она понижается и только от 50 до 100 °C повышается. Значит, удельная теплоёмкость воды достигает минимального значения при 36—37 °C, т. е. вблизи нормальной температуры тела человека и млекопитающих, благоприятной для биохимических реакций в их организме.
Ещё одна особенность воды — высокое поверхностное натяжение.
На каждую молекулу внутри жидкости действуют силы притяжения соседних молекул, окружающих её со всех сторон. На молекулы поверхностного слоя действуют как молекулы жидкости, так и молекулы газов воздуха. Взаимное притяжение молекул жидкости больше, чем молекул жидкости и газа, поэтому равнодействующая сил притяжения направлена внутрь жидкости и молекулы поверхностного слоя стремятся в неё втянуться. Под действием этой силы число молекул на поверхности уменьшается, её площадь сокращается. Но все молекулы, разумеется, не могут уйти внутрь. На поверхности остаётся такое их число, при котором она оказывается минимальной. Для перенесения молекул из глубины объёма жидкости в её поверхностный слой необходимо совершить работу по преодолению равнодействующей сил притяжения, действующих на молекулу в поверхностном слое. Материал с сайта http://doklad-referat.com
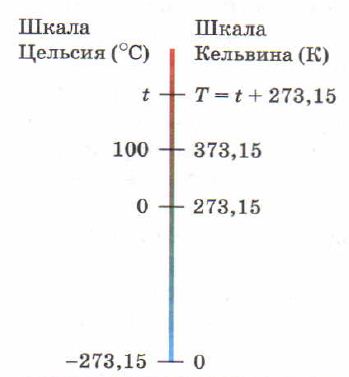 |
| Рис. 159. Температурные шкалы Кельвина и Цельсия |
 |
| Рис. 160. Капли росы стремятся принять форму шара |
 |
| Рис. 161. Водомерка |
Поверхностным натяжением называется величина, равная работе, затраченной на увеличение поверхности жидкости на одну единицу.
Поверхностное натяжение собирает воду в капли (рис. 160) и позволяет водомерке (рис. 161) скользить по воде.
Ещё одна характеристика воды — вязкость. Обычно с повышением давления вязкость вещества увеличивается, а с ростом температуры уменьшается. Вода и здесь выделяется. Её вязкость с ростом давления при температуре ниже -30 °C значительно уменьшается. Поэтому активность организмов, живущих в низкотемпературных средах, не сильно зависит от этих температур: кровь, не потерявшая текучести, продолжает выполнять свои функции столь же интенсивно, как и при более высоких температурах.
 На этой странице материал по темам:
На этой странице материал по темам:
Физ свойства воды аномалии-реферат
Перечислите известные аномалии физических свойств
При обычных условиях вода это жидкое прозрачное вещество
Аномальные свойства воды реферат по биологии кратко
Опыты для реферата с водой
 Вопросы по этому материалу:
Вопросы по этому материалу:
Какими физическими свойствами обладает вода?
Что такое поверхностное натяжение?
Как водородная связь определяет физические свойства воды?
Перечислите известные вам аномалии физических свойств воды.
Какую роль аномалии физических свойств воды играют в природе?





